ABSTRACT
Objective: To evaluate the health-related quality of life (HRQoL) of children/adolescents with asthma and that of their caregivers, comparing the two. Methods: This was a systematic review and meta-analysis based on the criteria of Preferred Reporting Items for Systematic Reviews and Meta-Analyses, with a strategy of searching five health-related databases (MEDLINE/PubMed, EMBASE, ScienceDirect, SciELO, and LILACS). We included studies that evaluated the HRQoL of children/adolescents with asthma and that of their caregivers with the Pediatric Asthma Quality of Life Questionnaire and the Pediatric Asthma Caregiver's Quality of Life Questionnaire, respectively, using the total scores and the scores on the domains activity limitation, symptoms (children/adolescents only), and emotional function. Results: We identified 291 articles, and we evaluated 133 of those. A total of 33 articles, collectively including 4,101 subjects, were included in the meta-analysis. An analysis stratified by study design showed no differences between the HRQoL of the caregivers and that of the children/adolescents in the activity limitation domain and in the total score. However, the mean emotional function domain scores were significantly higher (better) among children/adolescents with asthma than among their caregivers in longitudinal studies-Δ = 0.82 (0.21-1.44)-and randomized clinical trials-Δ = 0.52 (0.29-0.79)-although not in cross-sectional studies-Δ = −0.20 (−0.03 to 0.43). Conclusions: The total HRQoL scores proved to be similar between children/adolescents with asthma and their caregivers. However, the two groups differed in their perception of their emotional function, the caregivers scoring significantly lower than the children/adolescents in that domain.
Keywords:
Asthma; Quality of life; Surveys and questionnaires.
RESUMO
Objetivo: Avaliar e comparar os níveis de qualidade de vida relacionada à saúde (QVRS) de crianças/adolescentes com asma e de seus cuidadores. Métodos: Revisão sistemática e meta-análise baseada nos critérios de Preferred Reporting Items for Systematic Reviews and Meta-Analyses, com estratégia de busca em cinco bases de dados em saúde (MEDLINE/PubMed, EMBASE, ScienceDirect, SciELO e LILACS). Foram incluídos estudos que avaliaram a QVRS de crianças/adolescentes com asma e de seus cuidadores por meio dos escores totais e dos domínios limitação de atividades, sintomas (somente crianças/adolescentes) e função emocional do Pediatric Asthma Quality of Life Questionnaire e do Pediatric Asthma Caregiver's Quality of Life Questionnaire, respectivamente. Resultados: Do total de 291 artigos identificados, 133 foram avaliados e 33 foram incluídos na meta-análise, totalizando 4.101 sujeitos. A análise estratificada por tipo de delineamento não mostrou diferenças entre a QVRS de cuidadores e de crianças/adolescentes no domínio limitação de atividades e no escore total. Contudo, houve diferenças das médias no domínio função emocional em estudos longitudinais e ensaios clínicos randomizados - estudos transversais: Δ = −0,20 (−0,03 a 0,43); estudos longitudinais: Δ = 0,82 (0,21-1,44); e ensaios clínicos randomizados: Δ = 0,52 (0,29-0,79) - sendo que os cuidadores apresentaram menores escores que as crianças/adolescentes com asma. Conclusões: Os escores da QVRS entre cuidadores e crianças/adolescentes com asma demonstraram ser semelhantes quanto aos escores totais, mas divergiram na percepção das limitações emocionais, visto que os cuidadores apresentaram escores significativamente menores que as crianças/adolescentes nesse domínio.
Palavras-chave:
Asma; Qualidade de vida; Inquéritos e questionários.
INTRODUÇÃOA asma é uma doença inflamatória crônica que acomete indivíduos de todas as idades, principalmente crianças. É considerada um problema mundial de saúde, acometendo 300 milhões de pessoas no mundo,(1) e estima-se haver aproximadamente 20 milhões de asmáticos no Brasil. Na faixa etária pediátrica a prevalência de asma é de 20%.(2,3)
As repercussões da asma não são somente para o paciente, mas também para os pais e familiares. Ao longo do tempo, pode trazer implicações e problemas complexos que irão interferir negativamente na qualidade de vida (QV) de crianças, adolescentes, seus pais e familiares.(4)
O World Health Organization Quality of Life Group definiu QV como "a percepção que o indivíduo tem de si mesmo, da sua posição na vida, no contexto de cultura e sistema de valores nos quais ele vive e em relação às suas metas, expectativas e padrões sociais".(5) Assim, para compreender o completo estado de saúde da criança, é necessário, além da avaliação dos índices clínicos convencionais, verificar a QV relacionada à saúde (QVRS).(6)
A experiência dos pais e familiares tem um papel importante na QV de crianças e adolescentes asmáticos. A forma como o tratamento é recebido e conduzido é determinante para o controle adequado da doença.(7,8) No processo de cuidar da saúde da criança ou adolescente asmático, os pais e familiares devem ter uma percepção correta do processo de adoecimento.(9)
As doenças crônicas das crianças e adolescentes afetam negativamente a função familiar e a QVRS. Envolvem os pais e familiares com preocupações e responsabilidades quanto a necessidades de saúde da criança e do adolescente, serviços educacionais e médicos, custos da doença, perda de oportunidades sociais e ausências no trabalho, além de problemas físicos e emocionais.(10)
Nesse contexto, o presente estudo objetivou realizar uma meta-análise sobre os níveis de QVRS de crianças e adolescentes com asma e seus cuidadores.
MÉTODOSO estudo caracteriza-se por uma meta-análise, baseado nos critérios do Preferred Reporting Items for Systematic Reviews and Meta-Analyses,(11) sendo aplicada uma estratégia de pesquisa em cinco bases de dados em saúde para identificar os principais estudos que avaliaram os escores totais de controle da doença, bem como os de QVRS de pais e familiares de crianças com diagnóstico de asma.
Para fins de avaliação da QVRS das crianças/adolescentes com asma e seus cuidadores, foram incluídos estudos que avaliaram a QVRS dos asmáticos por meio dos escores totais do Pediatric Asthma Quality of Life Questionnaire (PAQLQ)(12) e de seus domínios limitação de atividades, sintomas e função emocional, assim como aqueles que avaliaram a QVRS dos pais e familiares (cuidadores) por meio dos escores totais do Pediatric Asthma Caregiver's Quality of Life Questionnaire (PACQLQ) e de seus domínios limitação de atividades e função emocional.(13) Como desfecho primário foi comparada a diferença entre os escores totais do PAQLQ e do PACQLQ, bem como a dos domínios limitação de atividades e função emocional.
Estratégia de buscaComo estratégia de busca foi adotada a lógica baseada em descritores específicos em inglês vinculados a operadores booleanos (AND e OR), com o auxílio de parênteses para delimitar intercalações dentro da mesma lógica e com o uso de aspas para a identificação de palavras compostas, aplicados da seguinte forma: (Asthma AND (PAQLQ OR "Pediatric Asthma Quality of Life Questionnaire") AND (PACQLQ OR "Pediatric Asthma Caregiver's Quality of Life Questionnaire"). As buscas foram aplicadas nas bases de dados PubMed (MEDLINE); EMBASE e ScienceDirect (Elsevier); e SciELO e LILACS (BIREME). As buscas foram realizadas em outubro de 2018, sem restrição de data limite das publicações.
Para evitar a inclusão excessiva de artigos, foram delimitadas as buscas nos seguintes campos: título (title), descritores (keywords) e resumo (abstract). Dessa forma, os descritores obrigatoriamente deveriam constar em pelos menos um dos três campos de busca, como, por exemplo, a busca efetuada na base de dados PubMed: (Asthma[Title/Abstract] OR Asthma[MeshTerms]) AND (PAQLQ[Title/Abstract] OR PAQLQ[MeshTerms] OR "Pediatric Asthma Quality of Life Questionnaire"[Title/Abstract] OR "Pediatric Asthma Quality of Life Questionnaire"[MeshTerms]) AND (PACQLQ[Title/Abstract] OR PACQLQ[MeshTerms] OR "Pediatric Asthma Caregiver's Quality of Life Questionnaire"[Title/Abstract] OR "Pediatric Asthma Caregiver's Quality of Life Questionnaire"[MeshTerms]). Além desses, não foram adicionados filtros para limitações, como, por exemplo, idioma do artigo ou público-alvo. Mediante a seleção dos potenciais artigos elegíveis para a revisão sistemática nas bases de dados em saúde, os arquivos foram exportados nos formatos (extensões) *.txt (MEDLINE), *.bib (BibiTeX) ou *.ris (RIS), contendo as seguintes informações: autores, título do artigo, descritores, periódico, ano, tipo de artigo e resumo.
Recrutamento, viés de seleção, critérios de inclusão e características dos estudosPara fins de recrutamento dos artigos potencialmente elegíveis para a revisão sistemática, após a exportação dos estudos selecionados nas bases de dados, utilizou-se o software específico para revisão sistemática StArt (State of the Art through Systematic Review), desenvolvido pelo Laboratório de Pesquisa em Engenharia de Software da Universidade Federal de São Carlos (São Carlos, SP, Brasil),(14) que serviu como base na identificação dos artigos previamente selecionados para a elaboração do fluxograma do estudo, contemplando quatro fases: a) Identificação: recrutamento dos estudos; b) Seleção: duplicidade e exclusão a partir da leitura dos títulos e resumos; c) Elegibilidade: exclusão a partir da leitura integral dos estudos; e d) Inclusão: inclusão dos estudos elegíveis, conforme critérios de inclusão pré-estabelecidos. Cada fase foi realizada separadamente por dois pesquisadores e analisada por um terceiro revisor, seguindo três critérios de inclusão ou exclusão dos artigos: artigos selecionados igualmente pelos dois pesquisadores foram incluídos; artigos não selecionados foram excluídos; artigos incluídos por apenas um pesquisador foram analisados pelo revisor que, no caso de enquadramento, foram incluídos. Para fins de inclusão de estudos por outros métodos (literatura cinzenta), foi adotado o critério de avaliação/inclusão a partir da leitura das referências (citações) dos estudos incluídos na fase de elegibilidade (leitura integral dos artigos).
Para sua inclusão na revisão sistemática, os artigos deveriam tratar-se de estudos transversais ou estudos em fases iniciais de estudos longitudinais, de caso-controle ou ensaios clínicos randomizados que abordassem como dados primários ou secundários os escores tanto dos domínios quanto dos escores totais do PAQLQ (crianças/adolescentes com asma) e do PACQLQ (cuidadores).(12,13) Estudos que, porventura, utilizaram outros instrumentos para avaliar a QVRS tanto de pais quanto de crianças/adolescentes foram excluídos.
Extração e apresentação dos dadosPara a extração dos dados para a identificação dos estudos elegíveis à revisão sistemática foram utilizadas tabelas pré-formatadas para registrar o autor principal, ano de publicação, local do estudo, delineamento, faixa etária dos asmáticos e sujeitos avaliados. Além disso, como critério de elegibilidade para a extração dos dados, foram considerados aqueles para a classificação da amostra: idade das crianças/adolescentes, sexo, etnia, gravidade e controle da asma, diagnóstico de rinite e/ou atopia, função pulmonar e fração de óxido nítrico exalado. Já para análise comparativa foram extraídos os domínios e o escore total do PAQLQ e do PACQLQ.(12,13)
A apresentação dos dados foi estruturada para demonstrar os valores quanto ao desenho de seleção dos estudos, características gerais dos estudos elegíveis (por autor e ano de publicação), características quanto ao perfil dos grupos estudados e quanto à comparação das médias ponderadas para os domínios limitação de atividades e função emocional, bem como para o escore total dos questionários de QVRS.
Análise estatísticaPara a realização da meta-análise, após a elegibilidade dos artigos e a identificação das variáveis de desfecho, utilizou-se o software Review Manager, versão 5.3 (RevMan 5; Cochrane Collaboration, Oxford, Reino Unido),(15) sendo aplicada a estatística randômica, com variância inversa da taxa de diferença média (bivariada), com IC95%, heterogeneidade (I2) e tamanho de efeito global e total (Z). O valor de significância foi de p < 0,05 tanto para a avaliação da pontuação média entre os escores totais, quanto à dos domínios da QVRS (intra e intergrupos) por tipo de delineamento: estudos transversais, longitudinais (de coorte) e ensaios clínicos randomizados.
Registro da revisão sistemáticaPara fins de registro da revisão sistemática, o estudo foi previamente cadastrado no International Prospective Register of Systematic Reviews (PROSPERO; Registro CRD42017081293).
RESULTADOSInicialmente foram identificados 129 artigos por meio das bases de dados em saúde - PubMed (n = 22); EMBASE (n = 55); ScienceDirect (n = 43); SciELO (n = 4); e LILACS (n = 5) - e 5 por meio de registros adicionados a partir da literatura cinzenta, totalizando 134 artigos. As exclusões ocorreram por duplicidade nas bases de dados (n = 9), falta de ajuste na leitura dos títulos e resumos (n = 78) e falta de enquadramento após a leitura integral do estudo (n = 13), restando 33 estudos elegíveis à meta-análise,(16-48) conforme o fluxograma na Figura 1.

Dos 33 artigos selecionados,(16-48) 28 (85%) foram publicados na última década, avaliando crianças e adolescentes (2-18 anos). Quanto ao delineamento dos estudos, 15 (45,4%) eram ensaios clínicos randomizados, 11 (33%) eram estudos transversais e 7 (21,2%) eram estudos longitudinais (de coorte). Quanto ao local de realização dos estudos, 17 (48%), 12 (36%), 4 (12%) e 1 (3%) eram provenientes dos continentes europeu, americano, asiático e africano, respectivamente (Tabela 1).

Na Tabela 2 são apresentados os valores ponderados dos 33 estudos selecionados para a revisão sistemática, totalizando uma amostra com 4.101 avaliações para o escore total, tanto de cuidadores (PACQLQ)(13) quanto de crianças/adolescentes com asma (PAQLQ).(12)

A Figura 2 apresenta a comparação dos níveis de QVRS entre cuidadores e crianças/adolescentes com asma para o domínio limitação de atividades, subdividido por tipo de delineamento. Foram avaliados 1.295 sujeitos (cuidadores/crianças) em 8 estudos transversais, apresentando uma heterogeneidade elevada (I2 = 97%) e tamanho de efeito total sem diferença estatística entre a pontuação média dos grupos (Z = 1,06; p = 0,290). Os 6 estudos longitudinais avaliaram 661 sujeitos, com heterogeneidade de I2 = 98% e Z = 0,07 (p = 0,940). Os 8 ensaios clínicos randomizados avaliaram 840 sujeitos e apresentaram heterogeneidade de I2 = 98% e Z = 0,96 (p = 0,340).

Esses resultados acabaram refletindo na média total ponderada, na qual a diferença total intergrupos demonstrou não haver distinção no domínio limitação de atividades entre 2.796 avaliações, com heterogeneidade intragrupo elevada (I2 = 98%; p < 0,001); homogeneidade intergrupo elevada, sem significância (I2 = 0%; p = 0,789); e tamanho de efeito global total baixo (Z = 1,81; p = 0,070).
A Figura 3 apresenta a comparação dos níveis de QVRS entre cuidadores e crianças/adolescentes com asma para o domínio função emocional, subdividido por tipo de delineamento. Em 8 estudos transversais foram avaliados 1.295 sujeitos no total, sendo a heterogeneidade elevada (I2 = 82%; p < 0,001) e o tamanho de efeito global baixo (Z = 1,73; p = 0,080). Nos 5 estudos longitudinais, que avaliaram 390 sujeitos, a heterogeneidade também foi elevada (I2 = 93%; p < 0,001), porém com diferença significativa entre as médias ponderadas (Δ = 0,82; IC95%: 0,213-1,44) para o grupo de crianças/adolescentes em relação ao de cuidadores, com um tamanho de efeito global elevado (Z = 2,61; p = 0,009). No entanto, os 7 ensaios clínicos randomizados, que avaliaram 806 sujeitos, apresentaram heterogeneidade semelhante à dos demais delineamentos (I2 = 82%; p < 0,001), com diferença estatística entre as médias ponderadas (Δ = 0,63; IC95%: 0,36-0,90) para o grupo de crianças/adolescentes em relação ao de cuidadores, o que refletiu no tamanho de efeito global (Z = 4,49; p < 0,001).
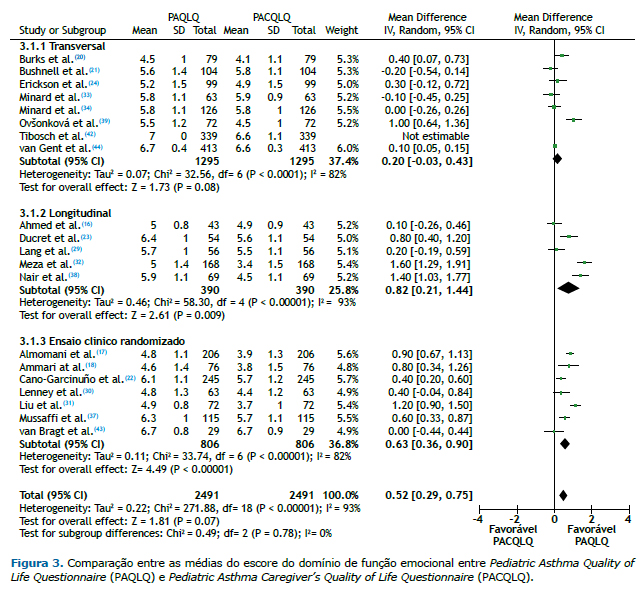
A média total ponderada entre as diferenças no domínio função emocional demonstrou haver redução nos escores para o grupo de cuidadores em relação ao de crianças/adolescentes com asma. Foram avaliados 2.491 sujeitos, com heterogeneidade de I2 = 93% (p < 0,001), mas com um tamanho de efeito global total moderado (Z = 4,52; p < 0,001), apresentando uma diferença estatisticamente significativa (Δ = 0,52; IC95%: 0,29-0,75) entre os dois grupos. Houve ainda heterogeneidade intergrupo moderada entre os subgrupos de delineamento, com I2 = 73,4% (p < 0,05), sendo que os estudos longitudinais apresentaram a maior média (Δ = 0,82; IC95%: 0,21-1,44), enquanto os transversais apresentaram a menor média (Δ = −0,20; IC95%: −0,03 a 0,43).
Por fim, na comparação da média ponderada dos escores totais da QVRS entre cuidadores e crianças/adolescentes com asma (Figura 4), envolvendo 4.101 sujeitos, os valores demonstram heterogeneidade intragrupo elevada quanto ao delineamento e tamanho de efeito total insignificante, refletindo na heterogeneidade total intergrupos (I2 = 96%; Δ = 0,03 [IC95%: −0,10 a −0,17]) e com tamanho de efeito global total de Z = 0,49 (p = 0,620).
 DISCUSSÃO
DISCUSSÃOA asma é uma doença crônica não transmissível, com elevado impacto de carga global, sendo responsável por elevadas taxas de absenteísmo escolar/ocupacional, visitas a emergências e hospitalizações, principalmente pela falta de diagnóstico médico adequado ou pela negligência do poder público quanto ao manejo da doença.(1)
A avaliação da QVRS de asmáticos e seus familiares vem ganhando destaque nas últimas duas décadas como parte integrante do manejo, tratamento e controle da doença. Para que haja efetividade no manejo da doença, além da adesão ao tratamento medicamentoso e o controle da sintomatologia da doença, a autopercepção dos escores de bem-estar físico, emocional e social acarretam grande impacto na vida, não somente dos acometidos pela doença, como também de seus familiares.(49)
A presente meta-análise teve como desenho de estudo a avaliação da QVRS por meio de instrumentos específicos, validados e com ampla aplicabilidade no meio científico em asma pediátrica, comparando domínios relacionados a limitações de atividade física e fatores emocionais, bem como os escores totais desses instrumentos, estratificando-os por tipo de delineamento. Os estudos longitudinais, bem como os ensaios clínicos randomizados, demonstraram que cuidadores apresentam menores escores relacionados a limitações emocionais que as crianças/adolescentes com asma, sendo que a maior diferença encontrada ocorreu entre as médias dos estudos longitudinais. Mesmo que não tenha sido demonstrada uma diferença significativa nos estudos transversais, a análise global manteve a magnitude dos resultados. Tais resultados corroboram a lógica de que os pais/cuidadores podem apresentar-se emocionalmente mais afetados do que as crianças pelo envolvimento com a carga de obrigações e de atenção aos filhos. Tal percepção pode variar conforme a idade da criança, sendo que pais/cuidadores de crianças mais jovens tendem a apresentar maiores efeitos em relação a esse domínio. (41,50,51) Em relação às limitações de atividades, não foram demonstradas diferenças significativas entre os escores de cuidadores e suas respectivas crianças/adolescentes. Estudos prévios(47,51) demonstram que os cuidadores tendem a subestimar as limitações de atividades dos asmáticos, influenciando na avaliação desse domínio. Também em relação aos escores totais, não foram evidenciadas diferenças entre os grupos.
Questionários de QVRS são ferramentas importantes para avaliar o estado de saúde de crianças/adolescentes com asma. No entanto, a concordância entre elas e seus cuidadores nas respostas tem se mostrado de baixa a moderada. Dos 33 estudos que preencheram os critérios de inclusão na presente revisão, 6 tiveram como objetivo correlacionar a QV de crianças e de seus cuidadores.(16,33,38,39,47,52) Nair et al.(38) correlacionaram a QV de crianças asmáticas e seus pais com o tratamento. Em 69 crianças (7-17 anos), após o tratamento, não foram verificadas alterações nos escores do domínio função emocional do PAQLQ, e cuidadores falharam em entender os efeitos psicológicos da asma nas crianças/adolescentes. Além disso, o tratamento não alterou os escores do PACQLQ.
Minard et al.(33) realizaram um estudo com 63 crianças (7-17 anos) comparando as versões originais dos questionários com sua versões eletrônicas e também correlacionando os questionários de QV das crianças/adolescentes com os dos cuidadores, demonstrando a validade das versões eletrônicas e a relação entre crianças/adolescentes e cuidadores. Além disso, não foram verificadas alterações no que diz respeito a atividades e sintomatologia.
Burks et al.(20) analisaram a concordância entre crianças/adolescentes asmáticas e seus cuidadores nos questionários em 79 pacientes (5-17 anos). Os escores apresentaram-se semelhantes, com correlação moderada entre função emocional e QV geral; no entanto, para o domínio limitação de atividades, os cuidadores subestimaram as crianças/adolescentes, que apresentaram escores mais altos do que os atribuídos pelos cuidadores (4,62 vs. 3,49; p < 0,001), sugerindo que crianças/adolescentes e cuidadores devem ser avaliados em relação a parâmetros de QV, não somente os cuidadores.
Outro estudo(16) com 43 crianças/adolescentes de 7-16 anos de idade com vários níveis de gravidade da asma demonstrou que meninas apresentam maior impacto no domínio limitação de atividades, bem como crianças/adolescentes com asma grave ou não controlada. Também se demonstrou uma correlação significativamente positiva entre o escore total de QV e o domínio função emocional (4,98 vs. 4,86; p = 0,015). Williams e Williams(47) encontraram baixa correlação entre os escores totais das crianças/adolescentes e de seus cuidadores (r = 0,19; p = 0,18), bem como com a avaliação de controle dada pelos clínicos assistentes (r = 0,02; p = 0,98). Houve também uma baixa correlação dos escores do domínio limitação de atividades entre as crianças/adolescentes e os cuidadores (r = 0,01; p = 0,45), sendo que as crianças/adolescentes reportaram menor limitação do que os cuidadores (4,8 vs. 4,1). Szabó et al.(41) demonstraram que cuidadores de crianças/adolescentes asmáticas possuem ao menos sintomas depressivos leves e tendem a ter maiores sintomas de ansiedade.
A presente meta-análise demonstrou valores altos de heterogeneidade entre os estudos quando esses foram avaliados de acordo com seu delineamento (intragrupos). Como sempre, em revisões sistemáticas complexas os estudos apresentaram grande variabilidade. No caso da asma, por ser uma doença com prevalência heterogênea (2-33%) e de causa multifatorial, uma heterogeneidade elevada é esperada nesse tipo de estudo. Além disso, algumas relações, como o tipo de delineamento do estudo avaliado, gravidade da doença, localização geográfica e status socioeconômico, podem influenciar a heterogeneidade, elevando-a.
Ovsonková et al.(39) demonstraram que o grau de controle da asma tem influência estatisticamente significante na QV das crianças/adolescentes com asma e de seus cuidadores, sendo que quanto melhor a QV dos primeiros, melhor a QV dos responsáveis. Sobre a idade e o controle, Voorend-van Bergen et al.(45) avaliaram a aplicabilidade de um diário eletrônico (web-based diary) para crianças/adolescentes com idade entre 4 e 18 anos, sendo que, para crianças menores de 12 anos, o diário era preenchido por seus cuidadores. Nessa faixa etária, a mediana do escore do PACQLQ foi de 6,5; a média do escore do PAQLQ dos adolescentes foi um pouco mais baixa (6,2); e as crianças/adolescentes com asma bem controlada tiveram escores de PAQLQ e PACQLQ significativamente maiores do que daqueles com asma parcialmente ou não controlada (p < 0,001).(53)
Para a elaboração do presente estudo, foram tomados cuidados sugeridos para sua realização com o mínimo de vieses; contudo, algumas limitações podem ser destacadas. Os resultados do estudo foram medidos por ferramentas subjetivas, e, portanto, o viés de memória pode afetar as respostas aos questionários. A idade dos pacientes e o nível de escolaridade e de cultura podem ter interferido na compreensão dos questionários. Os estudos também apresentaram diferentes intervalos entre a aplicação dos questionários e de intervenções e não avaliaram o tempo despendido pelos cuidadores para os cuidados com seus assistidos; por exemplo, crianças com sintomas mais graves tendem a ter maior atenção e exigir mais tempo dos cuidadores.(37)
Por fim, a presente meta-análise evidenciou claramente que a asma pode influenciar os escores de QV relacionados ao domínio função emocional de cuidadores e de crianças/adolescentes asmáticos com diferenças entre as percepções dos indivíduos. Porém, escores relacionados ao domínio limitação de atividades e escore total não apresentaram diferenças entre os grupos. Assim, os autores enfatizam a importância do acompanhamento adequado dessa população, com ênfase no estado emocional de todos os envolvidos (crianças, familiares e pessoas ao seu redor), mantendo o alerta para as interferências psicoemocionais relacionadas à asma.
REFERÊNCIAS1. Global Initiative for Asthma (GINA) [homepage on the Internet]. Bethesda: GINA; c2017 [cited 2018 Mar 6]. 2017 GINA Report Global Strategy for Asthma Management and Prevention. Available from: http://ginasthma.org/2017-gina-report-global-strategy-for-asthma-management-and-prevention/
2. Solé D, Camelo-Nunes IC, Wandalsen GF, Pastorino AC, Jacob CM, Gonzalez C, et al. Prevalence of symptoms of asthma, rhinitis, and atopic eczema in Brazilian adolescents related to exposure to gaseous air pollutants and socioeconomic status. J Investig Allergol Clin Immunol. 2007;17(1):6-13.
3. Roncada C, de Oliveira SG, Cidade SF, Sarria EE, Mattiello R, Ojeda BS, et al. Burden of asthma among inner-city children from Southern Brazil. J Asthma. 2016;53(5):498-504. https://doi.org/10.3109/02770903.2015.1108438
4. Nogueira KT. Avaliação da qualidade de vida entre adolescentes asmáticos [thesis]. Rio de Janeiro: Instituto de Medicina Social, Universidade do Estado do Rio de Janeiro; 2007.
5. The World Health Organization Quality of Life assessment (WHOQOL): position paper from the World Health Organization. Soc Sci Med. 1995;41(10):1403-1409. https://doi.org/10.1016/0277-9536(95)00112-K
6. Juniper EF. How important is quality of life in pediatric asthma? Pediatr Pulmonol Suppl. 1997;15:17-21. https://doi.org/10.1002/(SICI)1099-0496(199709)15+<17::AID-PPUL5>3.0.CO;2-O
7. Mandhane PJ, McGhan SL, Sharpe HM, Wong E, Hessel PA, Befus AD, et al. A child's asthma quality of life rating does not significantly influence management of their asthma. Pediatr Pulmonol. 2010;45(2):141-148. https://doi.org/10.1002/ppul.21157
8. Park M, Chesla CK. Understanding complexity of Asian American family care practices. Arch Psychiatr Nurs. 2010;24(3):189-201. https://doi.org/10.1016/j.apnu.2009.06.005
9. Payrovee Z, Kashaninia Z, Alireza Mahdaviani S, Rezasoltani P. Effect of Family Empowerment on the Quality of life of School-Aged Children with Asthma. Tanaffos. 2014;13(1):35-42.
10. Hockenberry MJ, Wilson D. Wong's nursing care of infants and children-E-book. Philadelphia: Elsevier Health Sciences; 2014.
11. Moher D, Liberati A, Tetzlaff J, Altman DG; PRISMA Group. Preferred reporting items for systematic reviews and meta-analyses: the PRISMA statement [published correction appears in Int J Surg. 2010;8(8):658]. Int J Surg. 2010;8(5):336-341. https://doi.org/10.1016/j.ijsu.2010.02.007
12. Elizabeth C, Suzanna S, Tim CF, Shek LP, Mital R, Bee Wah L. Pediatric asthma quality of life questionnaire: validation in children from Singapore [published correction appears in Asian Pac J Allergy Immunol. 2014;32(2):144. Chi, S L [corrected to Shek, L P] Bee-Wah, L [corrected to Bee Wah, L]]. Asian Pac J Allergy Immunol. 1999;17(3):155-161.
13. Stelmach I, Podlecka D, Smejda K, Majak P, Jerzyńska J, Stelmach R, et al. Pediatric asthma caregiver's quality of life questionnaire is a useful tool for monitoring asthma in children. Qual Life Res. 2012;21(9):1639-1642. https://doi.org/10.1007/s11136-011-0070-x
14. Srivastava SK. Green supply chain management: a state-of-the-art literature review. Int J Management Rev. 2007;9(1):53-80. https://doi.org/10.1111/j.1468-2370.2007.00202.x
15. Deeks JJ, Higgins JP. Statistical algorithms in review manager 5. Statistical Methods Group of The Cochrane Collaboration. 2010;1-11.
16. Ahmed PA, Ulonnam CC, Mohammed-Nafi'u R. Assessment of quality of life among children with bronchial asthma and their caregivers at the National Hospital Abuja, Nigeria. Niger J Paediatr. 2016;43(2):88-94. https://doi.org/10.4314/njp.v43i2.5
17. Almomani BA, Mayyas RK, Ekteish FA, Ayoub AM, Ababneh MA, Alzoubi SA. The effectiveness of clinical pharmacist's intervention in improving asthma care in children and adolescents: Randomized controlled study in Jordan. Patient Educ Couns. 2017;100(4):728-735. https://doi.org/10.1016/j.pec.2016.11.002
18. Ammari WG, Al-Hyari N, Obeidat N, Khater M, Sabouba A, Sanders M. Mastery of pMDI technique, asthma control and quality-of-life of children with asthma: A randomized controlled study comparing two inhaler technique training approaches. Pulm Pharmacol Ther. 2017;43:46-54. https://doi.org/10.1016/j.pupt.2017.02.002
19. Berger WE, Leflein JG, Geller DE, Parasuraman B, Miller CJ, O'Brien CD, et al. The safety and clinical benefit of budesonide/formoterol pressurized metered-dose inhaler versus budesonide alone in children. Allergy Asthma Proc. 2010;31(1):26-39.
20. Burks ML, Brooks EG, Hill VL, Peters JI, Wood PR. Assessing proxy reports: agreement between children with asthma and their caregivers on quality of life [published correction appears in Ann Allergy Asthma Immunol. 2013;111(4):309]. Ann Allergy Asthma Immunol. 2013;111(1):14-19. https://doi.org/10.1016/j.anai.2013.05.008
21. Bushnell DM, Martin ML, Parasuraman B. Electronic versus paper questionnaires: a further comparison in persons with asthma. J Asthma. 2003;40(7):751-762. https://doi.org/10.1081/JAS-120023501
22. Cano-Garcinuño A, Díaz-Vázquez C, Carvajal-Urueña I, Praena-Crespo M, Gatti-Viñoly A, García-Guerra I. Group education on asthma for children and caregivers: a randomized, controlled trial addressing effects on morbidity and quality of life. J Investig Allergol Clin Immunol. 2007;17(4):216-226.
23. Ducret CB, Verga M, Stoky-Hess A, Verga J, Gehri M. Impact d'une école de l'asthme sur la consommation en soins et la qualité de vie des enfants âgés de 4 à 12 ans et de leurs parents. Arch Pediatr. 2013;20(11):1201-1205. https://doi.org/10.1016/j.arcped.2013.08.021
24. Erickson SR, Munzenberger PJ, Plante MJ, Kirking DM, Hurwitz ME, Vanuya RZ. Influence of sociodemographics on the health-related quality of life of pediatric patients with asthma and their caregivers. J Asthma. 2002;39(2):107-117. https://doi.org/10.1081/JAS-120002192
25. Fleming L, Murray C, Bansal AT, Hashimoto S, Bisgaard H, Bush A, et al. The burden of severe asthma in childhood and adolescence: results from the paediatric U-BIOPRED cohorts [published correction appears in Eur Respir J. 2017;49(6):]. Eur Respir J. 2015;46(5):1322-1333. https://doi.org/10.1183/13993003.00780-2015
26. Halterman JS, Riekert K, Bayer A, Fagnano M, Tremblay P, Blaakman S, et al. A pilot study to enhance preventive asthma care among urban adolescents with asthma. J Asthma. 2011;48(5):523-530. https://doi.org/10.3109/02770903.2011.576741
27. Juniper EF, Gruffydd-Jones K, Ward S, Svensson K. Asthma Control Questionnaire in children: validation, measurement properties, interpretation. Eur Respir J. 2010;36(6):1410-1416. https://doi.org/10.1183/09031936.00117509
28. Kamps AW, Brand PL, Kimpen JL, Maillé AR, Overgoor-van de Groes AW, van Helsdingen-Peek LC, et al. Outpatient management of childhood asthma by paediatrician or asthma nurse: randomised controlled study with one year follow up. Thorax. 2003;58(11):968-973. https://doi.org/10.1136/thorax.58.11.968
29. Lang JE, Hossain MJ, Lima JJ. Overweight children report qualitatively distinct asthma symptoms: analysis of validated symptom measures. J Allergy Clin Immunol. 2015;135(4):886-93.e3. https://doi.org/10.1016/j.jaci.2014.08.029
30. Lenney W, McKay AJ, Tudur Smith C, Williamson PR, James M, Price D, et al. Management of Asthma in School age Children On Therapy (MASCOT): a randomised, double-blind, placebo-controlled, parallel study of efficacy and safety. Health Technol Assess. 2013;17(4):1-218. https://doi.org/10.3310/hta17040
31. Liu Z, Qureshi K. Efficacy of an Asthma Self-management Education Intervention for Children (9-13 Years) with Asthma and Their Caregiver in Wuhan, China. J US-China Med Sci. 2016;13:117-128. https://doi.org/10.17265/1548-6648/2016.03.001
32. Meza ÉD, Puentes ÓUB, Blanc JPG, García MG, Halley PD, Duque CAT. Evaluación del control del asma y la calidad de vida de los niños y sus padres o cuidadores en un programa de atención integral del asma (Programa Asmaire Infantil). Rev Medica Sanitas. 2012;15(4):36-42.
33. Minard JP, Thomas N, Olajos-Clos J, Juniper EF, Jiang X, Jenkins B, et al. Burden Of Childhood Asthma: Relationship Between Pediatric And Caregiver Electronic Quality Of Life Questionnaires. ATS. 2011:A1435. https://doi.org/10.1164/ajrccm-conference.2011.183.1_MeetingAbstracts.A1435
34. Minard JP, Thomas NJ, Olajos-Clow JG, Wasilewski NV, Jenkins B, Taite AK, et al. Assessing the burden of childhood asthma: validation of electronic versions of the Mini Pediatric and Pediatric Asthma Caregiver's Quality of Life Questionnaires. Qual Life Res. 2016;25(1):63-69. https://doi.org/10.1007/s11136-015-1055-y
35. Moreira A, Delgado L, Haahtela T, Fonseca J, Moreira P, Lopes C, et al. Physical training does not increase allergic inflammation in asthmatic children. Eur Respir J. 2008;32(6):1570-1575. https://doi.org/10.1183/09031936.00171707
36. Murray CS, Foden P, Sumner H, Shepley E, Custovic A, Simpson A. Preventing Severe Asthma Exacerbations in Children. A Randomized Trial of Mite-Impermeable Bedcovers. Am J Respir Crit Care Med. 2017;196(2):150-158. https://doi.org/10.1164/rccm.201609-1966OC
37. Mussaffi H, Omer R, Prais D, Mei-Zahav M, Weiss-Kasirer T, Botzer Z, et al. Computerised paediatric asthma quality of life questionnaires in routine care. Arch Dis Child. 2007;92(8):678-682. https://doi.org/10.1136/adc.2006.111971
38. Nair S, Nair S, Sundaram KR. A prospective study to assess the quality of life in children with asthma using the pediatric asthma quality of life questionnaire. Indian J Allergy Asthma Immunol. 2014;28(1):13-18. https://doi.org/10.4103/0972-6691.134210
39. Ovsonková A, Plavnická I, Jeseňák M. The quality of life of parents and children with asthma bronchial. Osetřovatelství a porodní asistence. 2012;3(3):424-432.
40. Strunk RC, Bacharier LB, Phillips BR, Szefler SJ, Zeiger RS, Chinchilli VM, et al. Azithromycin or montelukast as inhaled corticosteroid-sparing agents in moderate-to-severe childhood asthma study. J Allergy Clin Immunol. 2008;122(6):1138-1144.e4. https://doi.org/10.1016/j.jaci.2008.09.028
41. Szabó A, Mezei G, Kovári E, Cserháti E. Depressive symptoms amongst asthmatic children's caregivers. Pediatr Allergy Immunol. 2010;21(4 Pt 2):e667-e673. https://doi.org/10.1111/j.1399-3038.2009.00896.x
42. Tibosch M, Reidsma C, Landstra A, Hugen C, Gerrits P, Brouwer M, et al. An asthma-related quality of life instrument is unable to identify asthmatic children with major psychosocial problems. Eur J Pediatr. 2010;169(12):1495-1501. https://doi.org/10.1007/s00431-010-1250-3
43. van Bragt S, van den Bemt L, Kievits R, Merkus P, van Weel C, Schermer T. PELICAN: a cluster-randomized controlled trial in Dutch general practices to assess a self-management support intervention based on individual goals for children with asthma. J Asthma. 2015;52(2):211-219. https://doi.org/10.3109/02770903.2014.952439
44. van Gent R, van Essen LE, Rovers MM, Kimpen JL, van der Ent CK, de Meer G. Quality of life in children with undiagnosed and diagnosed asthma. Eur J Pediatr. 2007;166(8):843-848. https://doi.org/10.1007/s00431-006-0358-y
45. Voorend-van Bergen S, Vaessen-Verberne AA, Landstra AM, Brackel HJ, van den Berg NJ, Caudri D, et al. Monitoring childhood asthma: web-based diaries and the asthma control test. J Allergy Clin Immunol. 2014;133(6):1599-605.e2. https://doi.org/10.1016/j.jaci.2013.10.005
46. Voorend-van Bergen S, Vaessen-Verberne AA, Brackel HJ, Landstra AM, van den Berg NJ, Hop WC, et al. Monitoring strategies in children with asthma: a randomised controlled trial. Thorax. 2015;70(6):543-550. https://doi.org/10.1136/thoraxjnl-2014-206161
47. Williams J, Williams K. Asthma-specific quality of life questionnaires in children: are they useful and feasible in routine clinical practice?. Pediatr Pulmonol. 2003;35(2):114-118. https://doi.org/10.1002/ppul.10206
48. Yun TJ, Jeong HY, Hill TD, Lesnick B, Brown R, Abowd GD, et al. Using SMS to provide continuous assessment and improve health outcomes for children with asthma. Proceedings of the 2nd ACM SIGHIT International Health Informatics Symposium; 2012 Jan; Miami FL, USA. ACM; 2012. p. 621-630. https://doi.org/10.1145/2110363.2110432
49. Schmier JK, Chan KS, Leidy NK. The impact of asthma on health-related quality of life. J Asthma. 1998;35(7):585-597. https://doi.org/10.3109/02770909809048961
50. Costa DD, Pitrez PM, Barroso NF, Roncada C. Asthma control in the quality of life levels of asthmatic patients' caregivers: a systematic review with meta-analysis and meta-regression. J Pediatr (Rio J). 2019;95(4):401-409. https://doi.org/10.1016/j.jped.2018.10.010
51. Guyatt GH, Juniper EF, Griffith LE, Feeny DH, Ferrie PJ. Children and adult perceptions of childhood asthma. Pediatrics. 1997;99(2):165-168. https://doi.org/10.1542/peds.99.2.165
52. Burks ML, Brooks EG, Hill VL, Peters JI, Wood PR. Assessing proxy reports: agreement between children with asthma and their caregivers on quality of life [published correction appears in Ann Allergy Asthma Immunol. 2013;111(4):309]. Ann Allergy Asthma Immunol. 2013;111(1):14-19. https://doi.org/10.1016/j.anai.2013.05.008
53. Kew KM, Carr R, Crossingham I. Lay-led and peer support interventions for adolescents with asthma. Co-chrane Database Syst Rev. 2017;4(4):CD012331. https://doi.org/10.1002/14651858.CD012331.pub2









