ABSTRACT
Objective: To identify and classify risk factors for venous thromboembolism (VTE) in hospitalized patients, as well as to evaluate medical practices regarding prophylaxis for the disease. Methods: An observational cross-sectional study, carried out between January and March of 2006, involving inpatients at three hospitals in the city of Manaus, Brazil. Risk stratification for VTE was based on the criteria established by the Brazilian Society of Angiology and Vascular Surgery and by the International Union of Angiology. Clinical, surgical and medication-related risk factors were analyzed. The statistical analysis of the data obtained was conducted, adopting an alpha error of 5% and 95% CI. Qualitative data were analyzed using the chi-square test, whereas quantitative data were analyzed using Student's t-test. Results: Of the 1,036 patients included (total number of admissions, 1,051), 515 (49.7%) were male, and 521 (50.3%) were female. A total of 23 risk factors for VTE were identified (total number of occurrences, 2,319). The stratified risk for VTE was 50.6%, 16.6% and 30.8% among the admissions of high-, moderate- and low-risk cases, respectively. In 73.3% of the admissions, nonpharmacological prophylaxis was not employed at any point during the study period. In 74% of those classified as high- or moderate-risk cases, no prophylactic medications were administered. Conclusions: This study showed that, in the population studied, risk factors were common and that prophylactic measures were not employed in patients prone to developing VTE and its complications.
Keywords:
Venous thromboembolism; Risk factors; Venous thrombosis/prevention & control.
RESUMO
Objetivo: Identificar e classificar os fatores de risco para tromboembolismo venoso (TEV) em pacientes internados, avaliando as condutas médicas adotadas para a profilaxia da doença. Métodos: Estudo observacional, de corte transversal no período de janeiro a março de 2006, envolvendo uma população de pacientes internados em três hospitais na cidade de Manaus (AM). A estratificação do risco para TEV foi feita com base nos critérios da Sociedade
Brasileira de Angiologia e Cirurgia Vascular e da International Union of Angiology. Foram avaliados variáveis sobre os fatores de risco clínicos, cirúrgicos e medicamentosos, assim como os métodos profiláticos para TEV. Os dados foram analisados estatisticamente, adotando-se um alfa de 5% e IC95%. Os dados qualitativos foram analisados
pelo teste do qui-quadrado e os dados quantitativos pelo teste t de Student. Resultados: Foram estudados 1.036 pacientes num total de 1.051 internações, sendo 515 (49,7%) homens e 521 (50,3%) mulheres. Um total de 23 de fatores de risco para TEV foram identificados (número total de eventos, 2.319). O risco estratificado para TEV foi de 50,6%, 18,6% e 30,8% das internações para risco alto, moderado e baixo, respectivamente. Em 73,3% das internações, não foram adotadas medidas profiláticas não-medicamentosas durante o período do estudo, e em 74% das internações que apresentavam risco moderado ou alto, não foram adotadas quaisquer medidas terapêuticas
medicamentosas. Conclusões: Este estudo evidenciou que, na população estudada, os fatores de risco foram frequentes e que medidas profiláticas não foram utilizadas para pacientes com riscos potenciais de desenvolverem TEV e suas complicações.
Palavras-chave:
Tromboembolia venosa; Fatores de risco; Trombose venosa/prevenção & controle.
IntroduçãoO tromboembolismo venoso (TEV) compreende a trombose venosa profunda (TVP) e sua consequência imediata mais grave, a embolia pulmonar (EP).(1) Em sua fase aguda, associa-se a alta probabilidade de complicações graves, muitas vezes fatais.(2)
Encontra-se EP em cerca de 50% dos pacientes com TVP documentada. Em pacientes com EP clinicamente sintomática e objetivamente diagnosticada, foi relatada TVP silenciosa em cerca de 70% dos casos, provavelmente porque tais pacientes apresentavam pouca deambulação.(3,4) A TVP é uma complicação comum em ambiente hospitalar, com incidência documentada em 33% dos pacientes com pelo menos 48 h de internação.(5) A EP aguda está associada a altas taxas de morbidade e mortalidade, principalmente em pacientes hospitalizados, nos quais estudos de necropsias têm mostrado taxas entre 9% e 21%.(6,7)
Segundo um autor,(8) a incidência estimada para a trombose venosa é de 0,6 casos por 1.000 habitantes/ano. Em um consenso europeu para prevenção do TEV, estimou-se uma incidência de 160 casos de trombose venosa e 60 casos de EP por ano, a cada 100.000 habitantes, nos países ocidentais.(9)
A prevenção de TEV tem sido negligenciada nos hospitais em pacientes com insuficiência cardíaca congestiva, DPOC, câncer e infecções. Mesmo em hospitais altamente conceituados, é possível se encontrar um misto de omissão e de ações carentes de efetividades.(10)
A instituição de profilaxia para EP na presença de situações reconhecidas de risco constitui-se em medida de custo efetivo,(11) é amplamente recomendada por comitês normativos internacionais(12) e tem como base grandes ensaios clínicos, duplo-cegos e controlados por placebo.(13-15) Embora bem embasada cientificamente, a prática de profilaxia para a EP permanece insatisfatória em hospitais gerais, estendendo-se entre 9% e 56% na maioria dos estudos.(16-18) Essa é uma condição clínica comumente desenvolvida em ambiente hospitalar e, por ser raramente pensada como hipótese diagnóstica, evolui com complicações graves e fatais. A morte por EP de pacientes de alto risco para TVP ocorre rapidamente; na maioria das vezes, antes que o diagnóstico seja suspeitado.(4)
Diante de tal problemática, é de suma importância que a equipe de saúde tenha conhecimento técnico-científico sobre a abordagem e o manejo adequado de pacientes com risco de desenvolver EP. O objetivo deste estudo, portanto, foi o de avaliar quantitativa e qualitativamente os fatores de riscos e as práticas profiláticas adotadas por profissionais da área médica em pacientes internados no âmbito hospitalar da cidade de Manaus, contribuindo assim para um melhor conhecimento do processo saúde-doença e, em decorrência, proporcionando uma assistência mais eficaz.
MétodosTrata-se de um estudo observacional de corte transversal, realizado no período de janeiro a março de 2006, no Hospital Maternidade Unimed Manaus (HMU), entidade da rede privada de saúde; Fundação Hospitalar Adriano Jorge (FHAJ), pertencente à rede pública, atendendo as mais diversas especialidades, sendo este ligado a Universidade do Estado do Amazonas e a outras instituições de ensino; e a Fundação Centro de Controle de Oncologia do Amazonas (FCECON), também da rede pública e centro de referência em atendimento oncológico. Todos estão localizados na cidade de Manaus (AM).
A população foi constituída de pacientes internados nos hospitais acima citados dentro do período de estudo. Foram incluídos no estudo todos os pacientes internados maiores de 18 anos, dispostos a participar da pesquisa. Para seleção da amostra foi utilizado os seguintes critérios de exclusão: ser menor de 18 anos; apresentar, no momento da admissão, o diagnóstico de TVP e EP; não estar em pleno gozo de suas faculdades mentais; não concordar em participar do estudo ou não assinar o termo de consentimento livre e esclarecido após orientações realizadas pelos pesquisadores; estar em uso de anticoagulantes devido a outras condições clínicas; apresentar contraindicações para o uso de heparina em doses profiláticas (sangramento ativo, acidente vascular cerebral hemorrágico, discrasias sanguíneas, cirurgia oftalmológica, neurocirurgia e pós-operatório de cirurgias obstétricas); e estar grávida.
Os pacientes foram divididos, conforme a clínica de internação, em clínicos e cirúrgicos, sendo considerado paciente cirúrgico todo aquele que já houvesse sido submetido a algum procedimento cirúrgico na internação no momento do estudo.
Utilizou-se a técnica de análise de prontuários e uso de questionários conforme roteiro previamente elaborado contendo variáveis sobre os fatores de risco clínicos, cirúrgicos e medicamentosos, assim como os métodos profiláticos para TEV.
A coleta de dados ocorreu no período de janeiro a março de 2006 e foi composta de dois momentos: No primeiro momento, ao ser admitido no hospital, os pacientes eram identificados, avaliados quanto aos critérios de inclusão, entrevistados (conforme questionário) e estratificados conforme risco para TEV; No segundo, depois de identificados e incluídos no estudo, foram acompanhados através da verificação dos prontuários até a alta/óbito ou no período máximo de três meses para a verificação das medidas profiláticas para TEV instituídas pelos profissionais médicos. Optamos por este período de 3 meses por acreditarmos que, após esta data, o estudo poderia ter seus resultados influenciados por mudanças nas condutas médicas, a partir do conhecimento dos objetivos propostos pela pesquisa.
Para definir o risco de cada paciente, utilizou-se a estratificação do risco para TEV com base nos critérios da Sociedade Brasileira de Angiologia e Cirurgia Vascular (SBACV)(19) e da International Union of Angiology de 2001.(20) Os fatores de risco considerados foram os seguintes: idade avançada, imobilização, cirurgias, história anterior de TEV, câncer, trombofilia, varizes, obesidade, infecção, trauma, gravidez e puerpério, tempo de cirurgia prolongado, anestesia com duração maior que 30 minutos, anestesia geral, uso de estrógenos, insuficiência cardíaca, acidente vascular cerebral, paralisia, doença respiratória grave, doença inflamatória intestinal, infarto do miocárdio, insuficiência arterial, quimioterapia, síndrome nefrótica, e uso de cateteres centrais.
Os dados foram analisados estatisticamente através do programa Statistical Package for the Social Sciences, versão 13.0 (SPSS Inc., Chicago, IL, EUA), adotando-se um alfa de 5% e IC95%. Os dados qualitativos foram analisados pelo teste do qui-quadrado e os dados quantitativos pelo teste t de Student.
O trabalho foi aprovado pelo Comitê de Ética e Pesquisa da FCECON.
ResultadosForam estudados 1.036 pacientes de um total de 1.051 internações, sendo 515 homens (49,7%) e 521 mulheres (50,3%). A idade dos pacientes variou entre 18 e 95 anos (média de 53,31 anos).
A FHAJ apresentou uma quantidade maior de pacientes internados e estudados. Naquele hospital, foram acompanhados 864 pacientes (82,2%). Na FCECON, o número de pacientes estudados foi de 162 (15,4%), enquanto que no HMU foram incluídos na pesquisa apenas 25 (2,4%). A pequena quantidade de pacientes em estudo no HMU foi decorrente do tipo de clientela atendida no mesmo, onde prevalecem as gestantes, que não foram incluídas neste estudo.
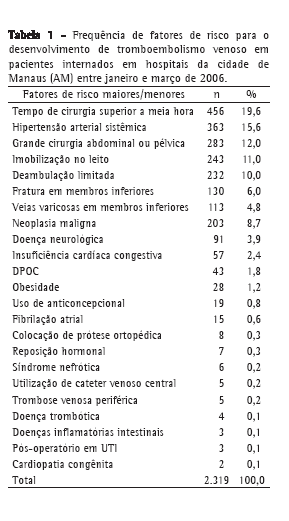
Foram identificados 2.319 fatores de riscos entre maiores ou menores, como mostra a Tabela 1, sendo o tempo de cirurgia superior a 30 minutos o risco mais prevalente (19,6%), seguido por hipertensão arterial sistêmica (15,6%). Dentre os fatores de risco destacamos, ainda, as grandes cirurgias abdominais e pélvicas (12%), a imobilização no leito (11%) e neoplasia maligna (8,7%).
O risco geral estratificado para TEV teve a seguinte distribuição: risco alto, 532 internações (50,6%); risco baixo, 324 (30,8%); e risco moderado, 195 (18,6%), conforme a Tabela 2.
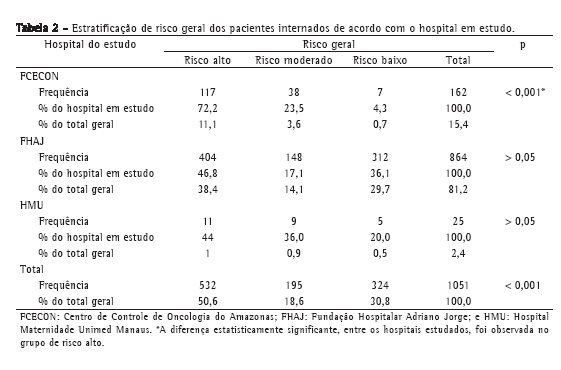
A FCECON foi o hospital com a maior proporção de pacientes com risco alto (72,2%; p < 0,001) conforme mostra a Tabela 2. A distribuição do risco na FHAJ foi de 404 internações de risco alto (48,6%), 148 de risco moderado (17,1%) e 312 de risco baixo (36,1%). No HMU, tivemos o seguinte resultado: 11 internações de alto risco (44%); 9 de risco moderado (36%) e 5 de risco baixo (20%).
Quando avaliamos os pacientes por tipo de clínica, observamos que não houve diferença estatisticamente significante na estratificação do tipo de risco entre as clínicas médica e cirúrgica, como mostra a Tabela 3.

Dos 727 pacientes com risco alto ou moderado, somente 189 (26%) foram submetidos a medidas profiláticas medicamentosas para o TEV.
Os clínicos fizeram uso de profilaxia medicamentosa com maior frequência que os cirurgiões (p < 0,001), e os cirurgiões utilizaram meios profiláticos não medicamentosos mais intensamente que os clínicos (p < 0,001), conforme se observa nas Tabelas 4 e 5. Verificou-se ainda que em 770 internações (73,3%) não foram adotadas medidas profiláticas não-medicamentosas de qualquer natureza.

 Discussão
DiscussãoA média de idade dos pacientes foi alta (53,31 anos), quando comparada com a de outros estudos.(1,21,22) Pacientes com mais de 40 anos têm um risco maior de desenvolver TEV e o risco dobra a cada década, a ponto de pacientes com mais de 75 anos terem um risco de TEV de 18,5%. Medidas profiláticas medicamentosas ou não-medicamentosas podem reduzir esse risco para 4,1%.(23) O TEV é uma importante causa de morbidade e mortalidade obstétrica, sendo que na gestante existe um risco 6 vezes maior de ocorrência do TEV, e a TVP incide em 1 a 2 casos por 1.000 gestações.(24-26)
Neste estudo, o risco geral estratificado para TEV mostrou um padrão diferente do de outros dois estudos realizados no Brasil(21,22), nos quais foram observadas prevalências de 52,43% e 39,91% para risco baixo, de 42,87% e 30,7% para risco moderado e de 4,7% e 29,39% para risco alto, respectivamente.
A FCECON foi o hospital com a maior proporção de pacientes com risco alto. Este fato se justifica pelas características da instituição, com o atendimento de pacientes oncológicos, o que proporciona uma maior probabilidade de ocorrência de eventos tromboembólicos, gerando um viés epidemiológico local. Pacientes com neoplasias apresentam um risco maior (RR entre 5 e 20) para o desenvolvimento de TEV.(27)
Pacientes com câncer em tratamento quimioterápico ou radioterápico tem aumentado de 3 para 6 vezes o risco de desenvolver TEV em relação à população normal.(28)
Dos 727 pacientes com risco alto ou moderado, somente 189 (26%) foram submetidos a medidas profiláticas medicamentosas para TEV. De acordo com as normas de orientações clínicas para prevenção da TVP da SBACV,(19) todos os pacientes com risco moderado e alto devem receber profilaxia medicamentosa, caso não haja contraindicação para o uso desta, e a profilaxia não-medicamentosa deve ser empregada em todo paciente internado, independentemente do risco para TEV.
Em um estudo realizado na Santa Casa de Misericórdia em Curitiba, obteve-se um resultado semelhante, pois somente 19,7% dos pacientes com risco moderado ou alto receberam este tipo de profilaxia.(22) Em um estudo realizado nos Estados Unidos com mais de 2.000 pacientes internados em 16 hospitais, mostrou-se que apenas um terço dos pacientes recebeu profilaxia apesar de apresentarem vários fatores de risco para TVP. Neste mesmo estudo, a profilaxia foi mais utilizada em hospitais escola.(23) Um comportamento em parte semelhante foi observado em nosso estudo, pois o Hospital Adriano Jorge, vinculado à Universidade do Estado do Amazonas, apresentou um percentual maior de uso da profilaxia medicamentosa (21,4%) em comparação aos outros hospitais estudados. Entretanto, em relação à utilização da profilaxia não-medicamentosa, não houve diferença estatisticamente diferente entre os
três hospitais estudados.
Os clínicos fizeram uso de profilaxia medicamentosa com maior frequência que os cirurgiões (p < 0,001), e os cirurgiões utilizaram meios profiláticos não-medicamentosos mais intensamente que os clínicos (p < 0,001). Uma possível explicação para a não-utilização da profilaxia medicamentosa para TEV em pacientes cirúrgicos é a preocupação dos cirurgiões quanto ao risco de sangramento durante a cirurgia que, teoricamente, o uso de anticoagulante pode acarretar. Contudo, dados de meta-análises e estudos randomizados duplo-cegos com placebo demonstraram não haver um aumento significativo de sangramento com o uso da heparina não fracionada em baixa dose e, principalmente, com o uso da heparina de baixo peso molecular.(29)
Outra explicação para a não-utilização da profilaxia medicamentosa é o alegado custo financeiro que ela pode acarretar. Porém, o seu uso, quando indicado corretamente, apresenta uma relação custo-benefício positiva.(30) Esta questão financeira, embora relevante na utilização adequada dos recursos, não é superior às necessidades do paciente do ponto de vista ético e científico. O que deve prevalecer sempre, na boa medicina, é o bem-estar do paciente.
Verificou-se que em 770 internações (73,3%) não foram adotadas medidas profiláticas não-medicamentosas (Tabela 5).
As medidas profiláticas não-medicamentosas consistem em medidas simples, como deambular, e devem ser aplicadas a todos os pacientes, inclusive os com baixo risco. Caso a condição clínica não permita ou inexista no serviço um sistema de compressão pneumática, a elevação dos membros inferiores que compense a diferença de altura em supino entre as veias da região poplítea e a veia femoral é considerada um método útil de prevenção do TEV em estudos não controlados e não acarreta nenhum ônus ao hospital.(23)
Como podemos observar, as medidas profiláticas são utilizadas em uma frequência abaixo da indicada, o que pode favorecer o aparecimento do EP, doença potencialmente fatal e merecedora da preocupação médica. As medidas profiláticas para os fenômenos tromboembólicos, apesar de serem bastante difundidas e terem sua eficácia comprovada, ainda necessitam atingir patamares bem mais adequados de utilização.
Neste estudo é importante destacar os seguintes aspectos: a) foi alta a prevalência de fatores de risco na população estudada; b) o percentual de fatores de risco estratificados em alto e moderado foi de 69,2% (727 internações); c) somente 26% dos pacientes que necessitavam de uma proteção medicamentosa receberam o tratamento. Enfim, este estudo evidenciou claramente que a profilaxia não estava sendo utilizada nos hospitais estudados, mesmo em pacientes com riscos potenciais de desenvolverem TEV e sua principal complicação, a EP.
Referências 1. Caiafa AS, Bastos M. Programa de profilaxia do tromboembolismo venoso do Hospital Naval Marcílio Dias: um modelo de educação continuada. J Vasc Bras. 2002;1(2):103-12.
2. Menna-Barreto S, Cerski MR, Gazzana MB, Stefani SD, Rossi R. Tromboembolia pulmonar em necropsias no Hospital de Clínicas de Porto Alegre, 1985-1995. J Pneumol. 1997;23(3):131-6.
3. Hirsh J, Hoak J. Management of deep vein thrombosis and pulmonary embolism. A statement for healthcare professionals. Council on Thrombosis (in consultation with the Council on Cardiovascular Radiology), American Heart Association. Circulation. 1996;93(12):2212-45.
4. Francis CW. Clinical practice. Prophylaxis for thromboembolism in hospitalized medical patients. N Engl J Med. 2007;356(14):1438-44.
5. Fedullo PF, Tapson VF. Clinical practice. The evaluation of suspected pulmonary embolism. N Engl J Med. 2003;349(13):1247-56.
6. Dismuke SE, Wagner EH. Pulmonary embolism as a cause of death. The changing mortality in hospitalized patients. JAMA. 1986;255(15):2039-42.
7. Lindblad B, Sternby NH, Bergqvist D. Incidence of venous thromboembolism verified by necropsy over 30 years. BMJ. 1991;302(6778):709-11.
8. Maffei FH. Epidemiologia da trombose venosa profunda e de suas complicações no Brasil. Cir Vasc Angiol. 1998;14:5-8.
9. Nicolaides AN, Arcelus J, Belcaro G, Bergqvist D, Borris LC, Buller HR, et al. Prevention of venous thromboembolism. European Consensus Statement, 1-5 November 1991, developed at Oakley Court Hotel, Windsor, UK. Int Angiol. 1992;11(3):151-9.
10. Goldhaber SZ, Turpie AG. Prevention of venous thromboembolism among hospitalized medical patients. Circulation. 2005;111(1):e1-3.
11. Collins R, Scrimgeour A, Yusuf S, Peto R. Reduction in fatal pulmonary embolism and venous thrombosis by perioperative administration of subcutaneous heparin. Overview of results of randomized trials in general, orthopedic, and urologic surgery. N Engl J Med. 1988;318(18):1162-73.
12. Geerts WH, Pineo GF, Heit JA, Bergqvist D, Lassen MR, Colwell CW, et al. Prevention of venous thromboembolism: the Seventh ACCP Conference on Antithrombotic and Thrombolytic Therapy. Chest. 2004;126(3 Suppl):S338-S400.
13. Cohen AT, Davidson BL, Gallus AS, Lassen MR, Prins MH, Tomkowski W, et al. Efficacy and safety of fondaparinux for the prevention of venous thromboembolism in older acute medical patients: randomised placebo controlled trial. BMJ. 2006;332(7537):325-9.
14. Leizorovicz A, Cohen AT, Turpie AG, Olsson CG, Vaitkus PT, Goldhaber SZ, et al. Randomized, placebo-controlled trial of dalteparin for the prevention of venous thromboembolism in acutely ill medical patients. Circulation. 2004;110(7):874-9.
15. Samama MM, Cohen AT, Darmon JY, Desjardins L, Eldor A, Janbon C, et al. A comparison of enoxaparin with placebo for the prevention of venous thromboembolism in acutely ill medical patients. Prophylaxis in Medical Patients with Enoxaparin Study Group. N Engl J Med. 1999;341(11):793-800.
16. Menna-Barreto SS, Faccin CS, Silva PM, Centeno LP, Gazzana MB. Estratificação de risco e profilaxia para tromboembolia venosa em pacientes internados em hospital geral universitário. J Pneumol. 1998;24(5):299-302.
17. Anderson FA Jr, Wheeler HB, Goldberg RJ, Hosmer DW, Forcier A, Patwardhan NA. Physician practices in the prevention of venous thromboembolism. Ann Intern Med. 1991;115(8):591-5.
18. Menna-Barreto SS, Silva PM, Faccin CS, Theil AL, Nunes AH, Pinehiro CT. Profilaxia para tromboembolia venosa em uma unidade de tratamento intensivo. J Pneumol. 2000;26(1):15-9.
19. Cabral AL, Silva MC, Barros Jr N, Castro AA, Santos ME. Normas de orientação clínica para o diagnóstico e tratamento da insuficiência venosa crônica. Belo Horizonte: Sociedade Brasileira de Angiologia e Cirurgia Vascular; 2001.
20. Nicolaides AN, Breddin HK, Fareed J, Goldhaber S, Haas S, Hull R, et al. Prevention of venous thromboembolism. International Consensus Statement. Guidelines compiled in accordance with the scientific evidence. Int Angiol. 2001;20(1):1-37.
21. Caiafa JS, de Bastos M, Moura LK, Raymundo S; Brazilian Registry of venous thromboembolism prophylaxis. Managing venous thromboembolism in Latin American patients: emerging results from the Brazilian Registry. Semin Thromb Hemost. 2002;28(Suppl 3):47-50.
22. Engelhorn AL, Garcia AC, Cassou MF, Birckholz L, Engelhorn CA. Profilaxia da trombose venosa profunda - estudo epidemiológico em um hospital escola. J Vasc Br. 2002;1(2):97-102.
23. Anderson FA Jr, Wheeler HB, Goldberg RJ, Hosmer DW, Patwardhan NA, Jovanovic B, et al. A population-based perspective of the hospital incidence and case-fatality rates of deep vein thrombosis and pulmonary embolism. The Worcester DVT Study. Arch Intern Med. 1991;151(5):933-8.
24. Garcia AA, Franco RF. Trombofilias adquiridas. In: Maffei FH, Lastória F, Yoshida WB, Rollo HA, editors. Doenças Vasculares Periféricas. Rio de Janeiro: MEDSI; 2002. p. 1397-405
25. Greer IA. Thrombosis in pregnancy: maternal and fetal issues. Lancet. 1999;353(9160):1258-65.
26. Silveira PR. Trombose venosa profunda e gestação: Aspectos etiopatogênicos e terapêuticos. J Vasc Bras. 2002;1(1):65-70.
27. Alvares F, Pádua AI, Terra-Filho J. Tromboembolismo pulmonar: diagnóstico e tratamento. Medicina. 2003;36(2/4):214-40.
28. Anderson FA Jr, Spencer FA. Risk factors for venous thromboembolism. Circulation. 2003;107(23 Suppl 1):I9-16.
29. Kakkar VV, Cohen AT, Edmonson RA, Phillips MJ, Cooper DJ, Das SK, et al. Low molecular weight versus standard heparin for prevention of venous thromboembolism after major abdominal surgery. The Thromboprophylaxis Collaborative Group. Lancet. 1993;341(8840):259-65.
30. Bick RL. Proficient and cost-effective approaches for the prevention and treatment of venous thrombosis and thromboembolism. Drugs. 2000;60(3):575-95.
Sobre os autores
Edson de Oliveira Andrade
Professor Associado de Clínica Médica. Universidade do Estado do Amazonas, Manaus (AM) Brasil.
Fábio Arruda Bindá
Acadêmico de Medicina. Universidade do Estado do Amazonas, Manaus (AM) Brasil.
Ângela Maria Melo da Silva
Acadêmica de Medicina. Universidade do Estado do Amazonas, Manaus (AM) Brasil.
Thais Ditolvo Alves da Costa
Acadêmica de Medicina. Centro Universitário Nilton Lins - Uninilton Lins - Manaus (AM) Brasil.
Marcélio Costa Fernandes
Acadêmico de Medicina. Universidade do Estado do Amazonas, Manaus (AM) Brasil.
Márcio Costa Fernandes
Acadêmico de Medicina. Universidade do Estado do Amazonas, Manaus
(AM) Brasil.
Trabalho realizado na Escola Superior de Saúde, Universidade do Estado do Amazonas, Manaus (AM) Brasil.
Endereço para correspondência: Edson de Oliveira Andrade. Rua Paraíba, Conjunto Abílio Nery, Quadra H, Casa 2, Adrianópolis, CEP 69057-021, Manaus, AM, Brasil.
Tel 55 92 3634-2171. E-mail: eandrade@vivax.com.br
Apoio financeiro: Este estudo recebeu apoio financeiro da Fundação de Amparo à Pesquisa no Estado do Amazonas (FAPEAM).
Recebido para publicação em 3/3/2008. Aprovado, após revisão, em 9/7/2008.








